Иммунитет – общебиологический феномен, суть которого заключается в долговременном самоподдержании внутри отдельного организма баланса между генетически «своим» и «не своим» в условиях чужеродного окружения.
Иммунная система – специализируется на реализации механизмов данного феномена
Иммунология – наука, изучающая защитные механизмы, направленные на устранение «не своего», и регуляторные процессы, которые формируют внутренний гомеостаз «своего» в организме.
Стратегическая функция иммунной системы: реализация генетической программы индивидуального развития организма от рождения до смерти в условиях чужеродного окружения.
Тактические функции иммунной системы:
- Защита от «не своего» (инфекция, трансплантат).
- Элиминация модифицированного своего (опухоли, поврежденные, стареющие клетки).
- Регуляция роста и развития клеток и тканей.
Нейро-иммунно-эндокринные взаимоотношения

Клиническая иммунология – это клиническая и лабораторная дисциплина, которая занимается обследованием, диагностикой и лечением больных с заболеваниями или патологическими процессами, развивающимися в результате нарушения иммунных механизмов, а также теми случаями, когда иммунологические манипуляции являются важной частью терапии и/или профилактики.
Выделяют четыре основные группы заболеваний, являющихся прерогативой клинической иммунологии:
- Связанные со снижением функции ИС – генетически обусловленным или приобретенным (так называемые иммунодефициты, в том числе СПИД);
- Развивающиеся в результате того, что специфические антитела и/или сенсибилизированные лимфоциты непосредственно сами или с помощью разных ассоциированных эффекторных систем приводят к повреждению тканей хозяина (аллергия и аутоиммунитет);
- Случаи, когда повреждение тканей хозяина может быть результатом действия ИС при защите хозяина против микроорганизмов (инфекция и иммунитет) или при отторжении органов и тканей;
- Заболевания, лечение которых включает применение иммуногенетики и иммунотропной терапии;
Таким образом, для реализации «клинической иммунологии» нужны не менее двух видов специалистов:
- Врачи, работающие с пациентами и непосредственно курирующие их (для взрослого и детского населения)
- Врачи, работающие в лаборатории
Врач-лаборант-иммунолог и клинический иммунолог обязаны работать рядом, в тесном контакте, а в идеале, быть взаимозаменяемыми и в диагностическом и, желательно, в лечебном процессе.
Все клетки, относящиеся к иммунной системе и привлекаемые ею для обеспечения эффекторных реакций, в функциональном отношении можно разделить на четыре группы:
- Антигенпрезентующие клетки
- макрофаги
- дендритные клетки
- В-лимфоциты
2. Регуляторные клетки
- Естественные регуляторные клетки (Tregs)
- Т-индукторы
- Т-хелперы 1, 2 и 3
- Т-регуляторы типа 1
3. Эффекторные клетки
- Плазматические клетки
- Цитотоксические Т-лимфоциты (CD8+)
- Эффекторные Т-клетки (CD4+)
- Нейтрофилы
- Моноциты/макрофаи
- Эозинофилы
- Базофилы
- Тучные клетки
- Натуральные киллеры
4. Клетки памяти
- Т-клетки памяти с фенотипом CD8+
- Т-клетки памяти с фенотипом CD4+
- Долгоживущие плазматические клетки
- В-клетки памяти
Главные идентификационные CD-маркёры клеток
| Обозначение кластера | Клетки |
| CD10, CD34 | Лимфоидная стволовая клетка |
| CD3 | T-лимфоцит |
| CD4 | Т-индуктор/Т-хелпер |
| CD8 | Цитотоксическая Т-клетка |
| CD19, CD72, CD79 и др. | B-лимфоцит |
| CD16/CD56 | NK-клетка |
| CD14, CD64 | Моноцит/макрофаг |
Молекулы иммунной системы могут быть условно разделены на пять групп. Рассмотрим более подробно морфологические и функциональные свойства двух основных популяций лимфоцитов, реализующих приобретенный (специфический) иммунитет.
Т-Лимфоциты
Итак, иммунологически незрелых стволовых клеток мигрирует из костного мозга в вилочковую железу (тимус), где под влиянием тимического микроокружения, прежде всего эпителиальных клеток и гормонов тимуса, созревают до иммунокомпетентных Т-лимфоцитов.
Созревание тимоцитов (незрелых лимфоцитов, попавших в тимус из костного мозга) происходит последовательно, по мере их перемещения из коркового слоя железы в мозговое вещество, т.е. из наружного слоя тимуса во внутренний.
У эмбриона человека тимус закладывается на 6-й неделе гестации и представляет собой эпителиальные клетки, окруженные мезенхимальной тканью. Лимфоидные клетки начинают определяться в тимусе человека на 13—14-й гестационной неделе. Тимус— источник Т-лимфоцитов; подсчитано, что у крыс массой 100 г он продуцирует за 1 ч ~ 20 млн. лимфоцитов.
Тимус созревает к 12—15 годам, после чего начинается так называемая физиологическая инволюция (возрастная, необратимая):
- уменьшается зона коркового вещества,
- снижается тимоцитопоэз,
- снижается продукция гормонов тимуса.
Различают также акцидентальную (обратимую), инволюцию тимуса:
- может развиться в любом возрасте (особенно это важно в младшем детском возрасте),
- под влиянием различных стрессовых воздействий (психоэмоциональных, экологических, лекарственных и др.).
Возрастная, также как и акцидентальная инволюция тимуса могут быть причиной развития вторичной иммунологической недостаточности.
Тимус продуцирует несколько гормонов, из них наиболее изучены следующие:
- Тимозин (фракция 5)
- Тимопоэтин — I и II
- Химический гуморальный фактор (ТГФ)
- Тимулин, или сывороточный химический фактор (СТФ)
Общим для всех перечисленных гормонов тимуса является их участие в процессах дифференцировки Т-лимфоцитов, возможно, на разных его этапах.
После окончания этапа антигеннезависимой дифференцировки в тимусе покоящиеся зрелые Т-лимфоциты, готовые к встрече с антигеном, через кровоток расселяются в определенных областях периферической лимфатической системы. Эти места получили название тимусзависимых зон (Т-зон) вторичных лимфоидных органов.
Тимусзависимые зоны (Т-зоны) вторичных лимфоидных органов:
- паракортикальная зона лимфатических узлов, богатая посткапиллярными венулами, обеспечивающими рециркуляцию лимфоцитов,
- периартериальные муфты лимфатических фолликулов селезенки (белая пульпа).
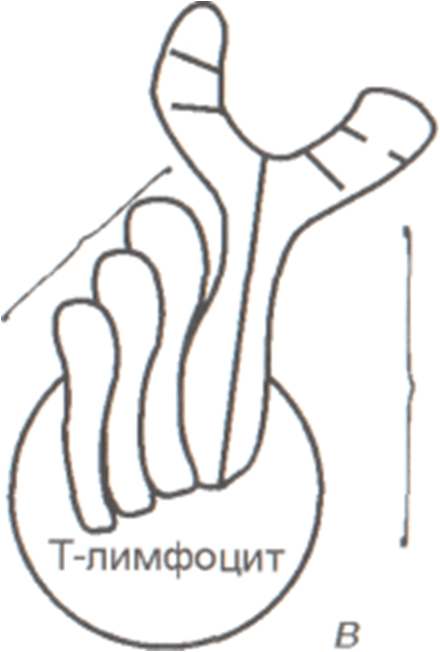
На поверхности всех Т-лимфоцитов имеется специальный инструмент, с помощью которого происходит распознавание чужеродного материала — Т-клеточный антигенраспознающий рецептор.
Т-клеточный антигенраспознающий рецептор имеется на мембране зрелых покоящихся Т-лимфоцитов, и не зависит от того, встречался ли ранее организм с данным антигеном или нет.
Встреча Т-лимфоцита со специфическим антигеном включает новый этап в жизни Т-лимфоцита— этап антигензависимой дифференцировки.
Распознавание специфического антигена приводит к активации Т-лимфоцита и последующей его пролиферации, заканчивающейся по явлением в организме большого количества (клона) Т-лимфоцитов определенной специфичности, способной реализовывать иммунный ответ.
Процесс распознавания чужеродного материала Т-лимфоцитом
Для распознавания крупной чужеродной (бактериальная, вирусная и другие клетки) или аутологичной структуры Т-лимфоцитам необходим промежуточный этап, на котором макрофаг или другая антигенпредставляющая клетка специальным образом “подготавливает” чужеродный материал для распознавания.
Этот процесс подготовки носит название процессинга (переваривания) и заключается в ферментативном расщеплении поглощенного макрофагом чужеродного материала.
Образующиеся в результате процессинга отдельные блоки (или пептиды), представляют собой определенной длины аминокислотные остатки — эпитопы чужеродного антигена. Именно эти пептиды и способны распознавать Т-лимфоциты в тот момент, когда они попадают на мембрану макрофага в сочетании с молекулами главного комплекса гистовместимости (ГКГ), или трансплантационными антигенами.
Т-лимфоциты относятся, в основном, к долгоживущей и медленно рециркулирующей популяции лимфоидных клеток. Есть данные о том, что длительность жизни для некоторых Т-лимфоцитов составляет 15— 20 лет.
Поскольку во взрослом состоянии заменяемость среди популяции Т-лимфоцитов невелика, то повреждения в этой части иммунной системы трудно восстанавливаются и имеют серьезные последствия.
Например удаление тимуса в период онтогенеза приводит к нарушению в иммунной системе. Это проявляется нарушением клеточных реакций организма и снижением продукции иммуноглобулинов (антител) на тимусзависимые антигены.
Например удаление тимуса в период онтогенеза приводит к нарушению в иммунной системе. Это проявляется нарушением клеточных реакций организма и снижением продукции иммуноглобулинов (антител) на тимусзависимые антигены.
На долю Т-лимфоцитов приходится (от общего числа лимфоцитов):
- в периферической крови — 55—75%,
- в селезенке — 60%,
- в лимфатическом узле — 70%.
Многообразие функций, которые выполняют Т-лимфоциты в рамках иммунного ответа организма, связано с существованием различных субпопуляций Т-лимфоцитов, “запрограммированных” на реализацию конкретной задачи в целях поддержания иммуногомеостаза.
Т-клетки подразделяют на две большие категории по их поверхностным гликопротеинам СD4 и СD8. Известно, что зрелые Т-клетки имеют только один из этих белков — либо СD4, либо СD8, но не оба. В отличие от этого, незрелые Т-лимфоциты, находящиеся в тимусе, могут быть одновременно СD4 – и СD 8 – положительными (двупозитивными – СD 4+ СО8+).
Молекулы СD4+ и СD8+ являются трансмембранными гликопротеинами и относятся к так называемым адгезивным молекулам.
Основные функции СD4+ и СD8+:
- участие в механизмах передачи сигнала внутрь лимфоцита в момент кооперации Т-лимфоцитов и антигенпредставляющих клеток при антигенном распознавании.
Обе субпопуляции Т-лимфоцитов относятся к так называемым иммунорегуляторным клеткам. От их соотношения в организме во многом зависит сила иммунного ответа. Соотношение иммунорегуляторных клеток генетически детерминировано и у каждого человека сугубо индивидуально (в среднем — 1,5—3,5).
СD4+ лимфоциты получили название Т-лимфоциты-хелперы/индукторы. Их количество в периферической крови достигает 55—60% от общего числа Т-лимфоцитов.
Основные функции СD4+ лимфоцитов:
- способствуют дифференцировке В-клеток в антителопродуцирующую плазматическую клетку;
- СВ8+ лимфоцитов — в зрелую цитотоксическую Т-клетку;
- макрофагам осуществлять эффекты гиперчувствительности замедленного типа.
Указанные функции СD4+ лимфоцитов реализуются за счет того, что они в свою очередь разделяются на две субпопуляции – Тh 1-го и 2-го типа, выполняющие разные хелперные функции за счет продукции цитокинов с разными функциями.
Тh1 и Тh2 различаются не только по способности продуцировать различные цитокины, но и по наличию на своей поверхности различных активационных маркеров. Обнаружено, что дисбаланс Тh1/Тh2 способствует развитию различных иммунопатологических реакций у человека.
Так, например, функция Тh1 преобладает при развитии множественного (рассеянного) склероза, инсулинозависимого сахарного диабета, аутоиммунного тиреоидита, болезни Крона, острого отторжения аллотрансплантата, привычного невынашивания плода и др.
Функция Тh2 преобладает при нормально протекающей беременности, трансплантационной толерантности, идиопатическом легочном фиброзе, прогрессирующем системном склерозе, у ВИЧ-инфицированных больных с быстрым прогрессированием заболевания, а также при аллергической патологии.
Таким образом, Т-лимфоциты-хелперы 1-го и 2-го типа представляют собой важнейшие субпопуляции Т-лимфоцитов, от функционального баланса которых зависит направленность иммунного ответа в норме и особенности клинических проявлений при развитии иммунопатологии.
СD8+ лимфоциты названы Т-лимфоцитами-киллерами/супрессорами (цитотоксическими лимфоцитами). Их содержание в периферической крови составляет 20—30%.
Другая субпопуляция Т-лимфоцитов, меньшая по количеству, несет на своей поверхности отличительный признак в виде молекулы СВ8 и относится, как уже упоминалось, к Т-лимфоцитам-киллерам/супрессорам. Такое двойное название означает, что эта субпопуляция Т-лимфоцитов может дифференцироваться либо в Т-киллер (цитотоксический Т-лимфоцит), либо в Т-супрессор и выполнять различные функции в зависимости от потребностей организма.
Основные функции CD8+:
- реализация специфических клеточных реакций иммунитета,
- участие в механизмах отторжения аллотрансплантатов,
- реакциях аутоиммунитета,
- разрушение вирусинфи-цированных и опухолевых клеток.
Таким образом, CD8+ — основная эффекторная клетка клеточно-опосредованного иммунитета, которая осуществляет лизис клеток- мишеней, обеспечивает генетическое постоянство внутренней среды организма.
В периферической крови и во вторичных лимфоидных органах CD8+ находится в состоянии покоя, – так называемая зрелая покоящаяся СD8+ клетка. Для того, чтобы произошла ее дифференцировка в зрелую клетку, способную осуществлять киллинговый эффект, требуется несколько условий.
- необходимо распознать чужеродный антиген;
- требуется время для создания клона специфических Т-киллеров, способных оказать ощутимый эффект.
Для распознавания чужеродного антигена у СD8+ клетки имеется ТАГ-рецептор в комплексе с СDЗ-молекулой. СD8+ клетка распознает не весь чужеродный антиген, а его блоки, так называемые доминантные пептиды, которые находятся на поверхности антигенпредставляющей клетки в сочетании с молекулами ГКГ.
Существует принципиальное различие в “работе” СD4+ клеток и СD8+ клеток при распознавании антигенов. Так, СD4+ Т-лимфоциты могут распознать чужеродный пептид только в том случае, если он презентируется в сочетании с молекулами гистосовместимости класса II на поверхности антигенпрезентирующей клетки. В норме в организме таких клеток немного — это моноциты-макрофаги, В-лимфоциты и дендритные клетки.
Совсем иначе осуществляется распознавание пептидов СD8+ Т-лимфоцитом. Основное отличие состоит в том, что патогенный пептид презентируется в составе молекулы гистосовместимости класса I, а не класса II, как для CD4+ Т-лимфоцитов.
Это очень важный момент, поскольку молекулы главного комплекса гистосовместимости класса I присутствуют на всех ядерных клетках организма.
Условие, необходимое для созревания СD8+ клеток: после распознавания чужеродного пептида эти клетки должны получить дополнительный сигнал от СD4+ клеток, который позволит им пролиферировать, в результате чего из одной клетки образуется клон клеток, обладающих одной специфичностью и достаточным потенциалом для реализации клеточного иммунного ответа.
Этапы “созревания“ СD8+ клеток при вирусной инфекции
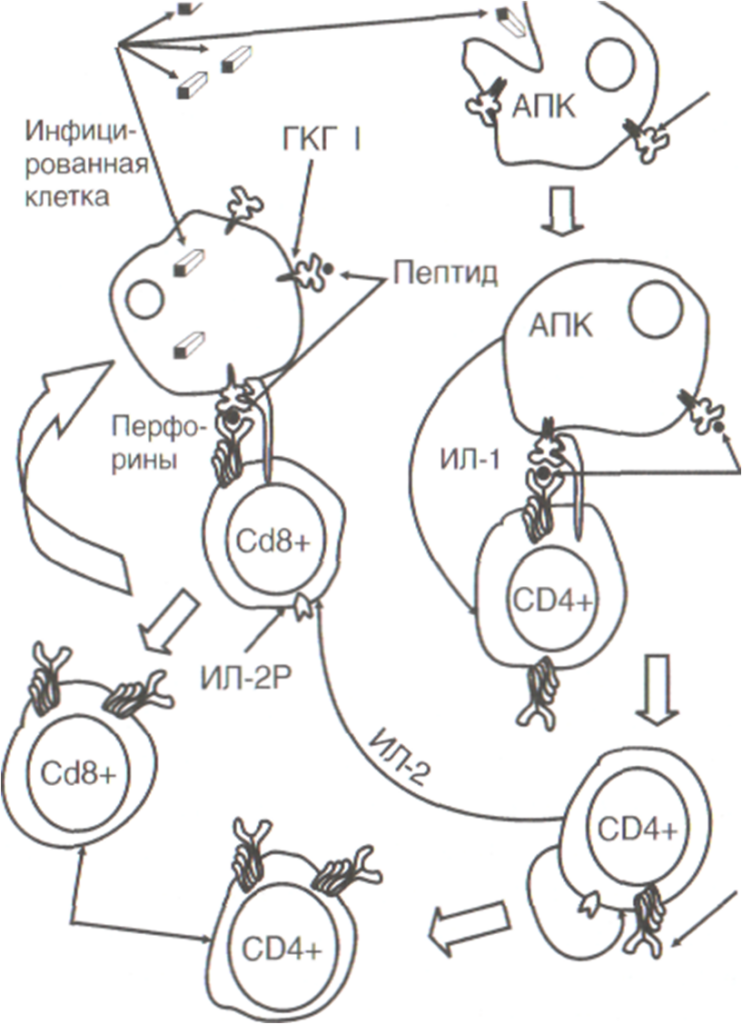
Среди Т-клеток существует несколько субпопуляций, несущих как СD4+, так и СD+ маркер, способных реализовать супрессорную или регуляторную функции. К ним отнесли Т-хелперы 3 типа (ТhЗ), продуцирующие факторы, обладающие супрессорным потенциалом.
В-лимфоциты
В-лимфоциты способны выполнять две важные функции:
- дифференцироваться в плазматические клетки и продуцировать антитела;
- выступать в роли антигенпредставляющих клеток.
В процессе эмбриогенеза стволовая клетка, из которой образуются В-лимфоциты, мигрирует в костный мозг, где и продолжает оставаться в течение всей жизни человека. В-лимфоциты образуются из стволовой клетки в костном мозге под влиянием костномозгового микроокружения и в отличие от Т-лимфоцитов не требуют для своего созревания прохождения через тимус.
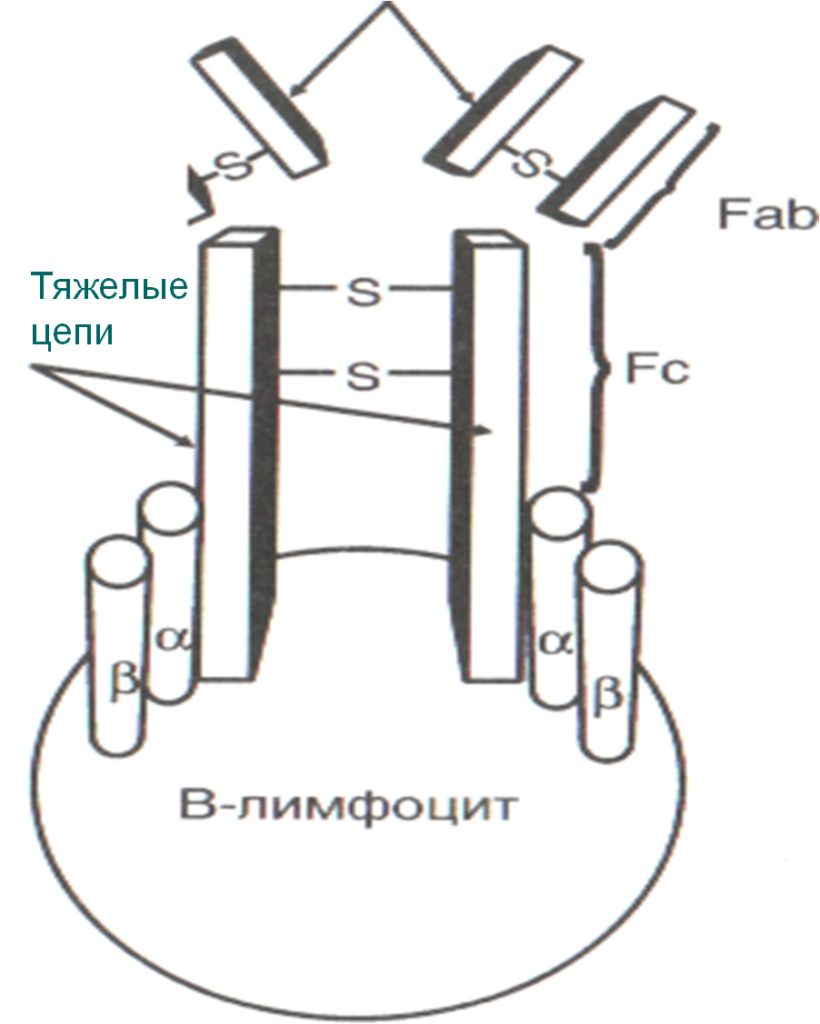
Созревание В-лимфоцитов происходит в две фазы:
Первая фаза — антигеннезависимая; проходит в костном мозге и заканчивается образованием зрелого покоящегося В-лимфоцита, отличительной особенностью которого является наличие на поверхности антигенраспознающего рецептора.
Он представляет собой мономерный IgМ, в отличие от циркулирующего в крови IgМ, который является пентамером. Строение В-клеточного антигенраспознающего рецептора традиционно для молекулы Ig и характеризуется наличием тяжелых и легких цепей, соединенных между собой дисульфидными мостиками.
Антигенраспознающий рецептор реагирует только с одним антигеном или с группой близкородственных антигенов. В организме каждого индивидуума имеется приблизительно 109 различных специфичностей В-лимфоцитов.
После связывания антигенов В-клетки активируются, начинают пролиферироватъ и формировать клон специфических плазматических клеток, с последующей секрецией специфических антител. Это приводит к накоплению этих антител в периферической крови. С этого момента начинается вторая фаза дифференцировки В-лимфоцитов — антигензависимая.
Т-независимая продукция антител
Независимая от СD4+ клеток стимуляция В-лимфоцитов — быстрый способ увеличения количества естественных антигенспецифических антител, представленных только одним классом иммуноглобулинов — IgМ.
Независимая от CD4+ Т-клеток-стимуляция В-лимфоцитов имеет следующие особенности:
- индуцируется за счет одновременного связывания большого числа В-клеточных антиген-распознающих рецепторов повторяющимися одинаковыми антигенными детерминантами возбудителя;
- не требует для активации В-клеток поглощения антигена и его процессинга.
К недостаткам такого иммунного ответа относится:
- продукция антител, принадлежащих только к одному классу иммуноглобулинов — IgМ;
- отсутствие иммунологической памяти. После одной-двух недель пролиферативная способность В-лимфоцитов снижается и секретирующие клетки погибают.
Т-зависимая продукция антител. В этом случае В-лимфоциты сначала функционируют как анти-Ig-представляющие клетки, а затем, дифференцируясь в плазматические клетки, как антителопродуцирующие.