F.R. Lillie (1912) впервые высказал мысль о том, что феномен оплодотворения есть
реакция антиген-антитело.
- Антиген МА-1 открывается при капацитации на внутренней поверхности супрануклеарной мембраны акросомы сперматозоида.
- На блестящей оболочке яйцеклетки для этого антигена содержится специфический рецептор.
- Трофобласт-лимфоцит перекрестно реагирующий антиген (TLX) – образуется в просвете эпителия семенных везикул и находится в семенной плазме.
- HLA-совместимость супругов.
Особенности иммуносупресссии при нормальной беременности
- Белок ранней фазы беременности.
- Антиген TLX.
- Отсутствие на трофобласте классических антигенов гистосовместимости класса I.
- Наличие на трофобласте антигенов HLA локуса G:
- отсутствие трофобласт-специфических Т-киллеров;
- созревание Т-супрессоров,
- подавление функции ЕК-клеток,
- регуляторная роль ЕК-клеток,
- супрессия функции макрофагов.
5. Барьерная функция плаценты.
6. Плацента как сорбент анти-НLА-антител.
7. Иммунорегуляторная роль плаценты:
- хорионический гонадотропин,
- плацентарный лактоген,
- трофобластический бета-1-гликопротеин
- прогестерон-индуцированный супрессивный фактор:
– подавляет функцию ЕК-клеток
– подавляет продукцию альфа ФНО
– усиливает функцию Th-2 типа
8. Онко-фетальный альфа2-фетопротеин.
9. Усиление функции Th-2 типа:
- интерлейкин 4,
- интерлейкин 10,
- усиливается продукция нецитотоксического Ig G1.
10. Снижение функции Th-1 типа:
- интерлейкин 2,
- гамма-интерферон,
- альфа-фактор некроза опухолей,
- снижается продукция цитотоксических Ig G2a.
К основным факторам, которые выработались в процессе эволюции для защиты полуаллогенного плода от иммунной системы матери, относятся следующие:
- Отсутствие на клетках трофобластаклассических антигенов HLA класса I и П.
- Сдвиг функционального баланса CD4+ Т-хелперов в сторону Тh-2типа.
- Иммунорегуляторная роль плаценты,обеспечивающая своеобразный иммуносупрессив-ный фон в организме матери.
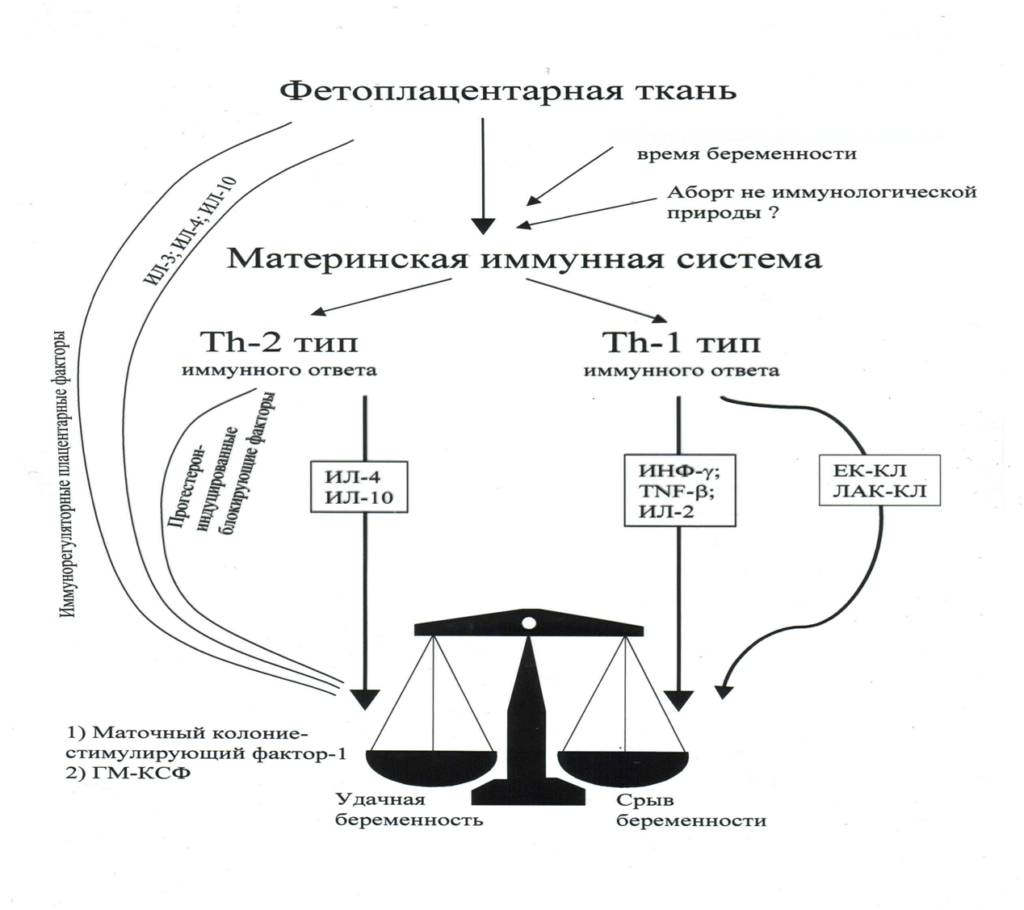
Особенности иммунных механизмов при иммунозависимых формах бесплодия.
- Повышение продукции гамма-интерферона:
- усиление функции ЕК-клеток, ЛАК-клеток,
- подавление секреции ГМ КСФ клетками эпителия матки,
- прямое повреждение клеток трофобласта.
2. Повышение продукции фактора некроза опухолей альфа:
- подавление пролиферации и дифференцировки клеток трофобласта,
- индукция гибели клеток трофобласта по механизмам апоптоза.
3. Одновременное повышение продукции -ИНФ, -ФНО и ИЛ-2 – прерывание беременности.
4. Снижение продукции ИЛ-4 и ИЛ-10.
5. Повышенная совместимость супругов по HLA-антигенам.
6. Вторичный иммунодефицит.
7. Антигаметный ауто (иммунный) конфликт.
Роль и место современной иммунологии в андрологии
- Исследование иммунных механизмов развития андрологической патологии.
- Лабораторная диагностика:
– выявление инфекционного агента;
– оценка иммунного статуса;
– выявление аутоиммунного компонента.
- Применение иммунотропных препаратов в комплексной терапии.
Спермальная функция
- Подвижность
- Пенетрация цервикальной слизи
- Акросомальная реакция
- Связывание с zona pellucida
- Пенетрация ZP
- Связывание с оолеммой (oolemma)
- Формирование проядра (pronucleus)
Механизмы развития антиспермального иммунитета
- Механическое, воспалительное, термическое и/или иное повреждение яичек.
- Нарушение целостности гематотестикулярного барьера.
- Контакт иммунокомпетентных клеток с аутоантигенами развивающихся сперматогенных клеток.
- Развитие сенсибилизации и продукция антиспермальных антител.
- Поражение контрлатерального органа аутоиммунным воспалением.
Роль перекрестных реакций между микроорганизмами и сперматозоидами.
- Фиксация на сперматозоидах Mycoplasma genitalis и Ureaplаsma urealyticum
-снижение подвижности сперматозоидов;
– нарушение капацитации;
– индукция аутоиммунных реакций.
2. Наличие Chlam. trach. сопровождается ухудшением количественных показателей спермограммы.
- Антиспермальные антитела выявляются только у ⅓ мужчин с инфекциями репродуктивного тракта.
Бесплодие – это отсутствие беременности в течение года супружеской (совместной) жизни без предохранения.
Условия, необходимые для зачатия:
- Мужчина должен продуцировать адекватное (необходимое) количество нормальных, подвижных сперматозоидов.
- Мужчина должен эякулировать сперму через неповрежденный семявыводной проток.
- Сперма (сперматозоиды) должна пройти (traverse) через необструктивный женский репродуктивный тракт.
- Женщина должна овулировать и выделить (высвободить) яйцеклетку.
- Оплодотворенная яйцеклетка должна быть способна развиваться и имплантироваться в соответственно подготовленный эндометрий.
Причины бесплодия
- Дефекты семени – 25%
- Трубный дефект – 22%
- Дефект овуляции – 27%
- Эндометриоз – 5%
- Другие – 4%
- Неясной этиологии – 17%
Анти-спермальные аутоантитела
- В 1955 году Rumke и Hellinga обнаружили ассоциацию между наличием анти-спермальных антител и бесплодием неясной этиологии.
- Последующие результаты были противоречивы, их объяснение было затруднено из-за разных методов определения.
- Гуморальные антитела не влияют на фертильность, если они не присутствуют в репродуктивном тракте.
- Антитела должны быть обнаружены на поверхности сперматозоидов.
- Спонтанная агглютинация.
- Подвижность\пенетрация
- присоединение к хвосту сперматозоида.
- Разрушение
- IgG опосредованная активация комплемента (хвост)
- семенная жидкость содержит ингибиторы комплемента, поэтому атака мембраны сперматозоида развивается в женском репродуктивном тракте
Анти-спермальные антитела у женщин
- Клинически значимы только при высоких титрах в сыворотке.
- Анти-спермальные антитела могут присутствовать в вагинальном секрете или цервикальной слизи даже когда гуморальные антитела не определяются.
Диагноз иммуно-зависимого бесплодия
- Пост-коитальный тест оценивает жизнеспособность сперматозоидов в цервикальной слизи.
- Гуморальные антитела.
- Ограниченная диагностическая ценность
- Обнаружение антител на поверхности сперматозоидов
Бесплодие неясной этиологии
При отсутствии зачатия или привычном прерывании в первые недели определяют степень сенсибилизации жены к антигенам мужа.
- Совместимость по HLA-антигенам.
- Антитела в сыворотке жены к лейкоцитам мужа.
- Однонаправленная смешанная культура лимфоцитов (one way MLC).
При отсутствии (слабой) сенсибилизации проводят иммуностимуляцию жены.
- В\к введение лейкоцитов мужа в дозе 50-100х106.
- В\в введение нормального Ig в дозе 0,5 мг\кг, разово.
При привычном прерывании беременности неясной этиологии (2-3 триместр) женщину обследуют на наличие антифосполипидных антител, анти-ядерных антител, антилейкоцитарных антител и количество ЕК клеток.
При выявлении антифосфолипидных антител, анти-ядерных антител и высоких титров антилейкоцитарных (к лейкоцитам мужа) антител и высокого количества ЕК-клеток назначают:
- в фолликулярной фазе до беременности, в\в, нормальный Ig, в дозе 500 мг\кг, разово.
далее каждіе 28 дней, в течение 4 месяцев. - Если беременность наступила – введение продолжают до родов или до 28-32 недели.
Лабораторная диагностика
1. Выявление инфекционного агента (ИФА, ПИФ, ПЦР и др.).
2. Оценка иммунного статуса (интегрального и местного):
- гуморальные факторы (Ig, sIg, C, s-ICAM);
- клеточные факторы (CD3, 4, 8, 22, 16, CD4+25+, CD54, 95, HLA-DR+);
- цитокины (ИЛ-1; 2; 4; 6; 10; ИНФ, ОНФ, ТФР- и их рецепторы);
- про- и анти-апоптические маркеры;
- неспецифические факторы (МфМн, Нф, лизоцим и др.);
- Типирование по HLA-антигенам.
3. Выявление аутоиммунного компонента:
- антиспермальные АТ (IgA, G, M);
- антипростатические АТ;
- клеточная сенсибилизация;
- белки теплового шока;
- антитела к белкам теплового шока.