Краш-синдром (синдром длительного сдавления тканей) — комплекс общих и местных изменений, наступающих в организме при длительном сдавлении мягких тканей, главным образом, мышц.
Первые описания такого рода патологии появились в германоязычной литературе после землетрясения в Мессине 1909 года, а в англоязычной литературе — с началом II Мировой войны в 1940 году, когда она и получила название краш-синдрома.
Синонимы
- Миоренальный синдром
- Травматический токсикоз,
- Синдром длительного раздавливания,
- Травматический рабдомиолиз,
- Синдром освобождения,
- Ишемический некроз мышц и т.д.
В международной классификации болезней МКБ-10 это состояние обозначено как «Т79.5 Травматическая анурия, синдром раздавливания, почечная недостаточность, сопровождающая размозжение».
Встречаемость
Краш-синдром относится к числу тяжелых форм патологии и нередко встречается в мирных условиях и военное время. Особенно часто наблюдается при землетрясениях, техногенных катастрофах, в том числе обвалах в шахтах. Ежегодно на земном шаре происходит около 25 крупных землетрясений, каждое из которых высвобождает энергию эквивалентную энергии взрыва 50 атомных бомб, сброшенных на Хиросиму.
Выживаемость
Существенной в развитии синдрома является и длительность сдавления: при кратковременном сдавлении (точнее раздавливании) шок возникает лишь при наличии костных повреждений. При извлечении из завалов не позднее получаса после катастрофы выживают более 99% пострадавших, при нахождении в завале в течение 1 суток — 81%, в течение 2, 4 и 5 суток — 33,7%, 19% и 7,4% соответственно (Sheng Z.Y., 1987).
В случае крайне тяжелых форм краш-синдрома гибель пострадавшего может наступить в первые–вторые сутки и без выраженных симптомов ОПН.
Позиционный синдром
- При длительном — от 6 часов и более — обездвиженном и фиксированном положении тела или конечностей пострадавшего возможно возникновение позиционного синдрома.
- Возникает у лиц, находящихся в бессознательном состоянии, являющемся результатом тяжелого отравления алкоголем и его суррогатами, наркотиками или снотворными препаратами, окисью углерода.
- Развитие позиционного синдрома после продолжительных операций под общим наркозом, после длительного нахождения шины на поврежденной конечности.
- Глубокая миорелаксация, способствующая пережатию сосудов и нарушению кровотока в конечностях.
- Анаэробная инфекция Clostridium oedematiens.
В патогенезе синдрома длительного сдавления наибольшее значение имеют 3 фактора:
- Болевое раздражение, вызывающее нарушение координации возбудительных и тормозных процессов в центральной нервной системе;
- Травматическая токсемия, обусловленная всасыванием продуктов распада из повреждённых тканей (мышц);
- Плазмопотеря, возникающая вторично в результате массивного отёка повреждённых конечностей.
Ишемия
- Краш-синдром развивается у пострадавших, у которых имелось сдавление тканей на протяжении не менее 4 часов (Michaelson M., 1992).
- Декомпрессия при экспериментальном краш-синдроме сопровождается прогрессированием деструктивных процессов в мышцах в результате повреждающего действия реперфузии. Если не допустить рециркуляции крови в конечности, животные под прессом не погибают.
- Дискретный, а не сплошной характер развивающегося в дальнейшем в зоне сдавления некроза мышц.
- Т.М. Оксман и М.В.Далин (1977) выделили из отчлененной конечности «ишемический токсин», обладающий выраженным вазоконстрикторным действием.
- Гипербарическая оксигенация позволяет во многих случаях сохранить поврежденную конечность и уменьшить выраженность интоксикации.
Боль
Продолжающийся, а не кратковременный характер воздействия на ткани, чем обусловлено то обстоятельство, что продолжительность эректильной фазы шока, по данным экспериментальных наблюдений, может достигать 1,5 часов. Это должно вести к более продолжительной гипоксии в органах, кровоснабжением которых организм жертвует в пользу других органов, более важных для поддержания жизнедеятельности в данный момент.
В условиях ацидоза болевые рецепторы теряют чувствительность, но это не значит, что после прекращения компрессии пострадавшие не испытывают болевых ощущений: они сохраняются, но уже за счет двух других факторов: за счет растяжения мышечных футляров при отеке мышц и за счет раздражения хеморецепторов в условиях накопления в тканях недоокисленных продуктов.
В эксперименте установлено, что уменьшение потока болевой импульсации путем новокаиновой блокады, денервации конечности или при сдавление под наркозом значительно повышает выживаемость животных как в период компрессии, так и в ближайшие часы посткомпрессионного периода, но не предотвращает развития краш-синдрома.
При введении животному мышечного экстракта, т.е. когда нет болевого фактора, краш-синдром не развивается. Однако при позиционном синдроме исход не лучше, хотя пострадавший находится в бессознательном состоянии.
Ацидоз
- В периоде компрессии в тканях, непосредственно подвергающихся сдавлению, и в находящихся более дистально за счет продолжительной ишемии происходит накопление недоокисленных продуктов обмена, главным образом, молочной и пировиноградной кислот, которые в дальнейшем, поступая в кровь, ведут к развитию метаболического ацидоза (Storgaard M. et al., 1998).
- Выраженность ацидоза зависит не столько от силы сдавления и даже не от площади сдавливаемого участка, сколько от продолжительности сдавления. Даже если артерии оказываются не полностью пережатыми, в тканях происходит нарушение оттока лимфы и крови, что ведет к нарушению притока артериальной крови, при этом поражение тканей происходит по аналогии с таковым при редко встречающемся патологическом состоянии — флегмазии или венозной гангрене.
- Значительное снижение рН крови некоторые исследователи считают ведущим фактором в развитии краш-синдрома
- В эксперименте показано, что рН венозной крови, составлявший 7,05 до компрессии, снижается к концу 6-го часа компрессии до 6,87, и становится еще ниже после декомпрессии. Это обстоятельство теоретически может влиять на патогенез ОПН за счет возникающего в связи с ацидозом спазма ветвей почечных артерий, в развитии которого при краш-синдроме может участвовать и болевой фактор.
Миоглобин
Миоглобин — хромопротеид с молекулярной массой 16114 Да. Как и гемоглобин, он способен связывать кислород и нужен для того, чтобы обеспечивать клетку заранее зарезервированным кислородом, когда в момент сокращения мышцы сосуды пережимаются.
Миоглобин обладает значительно более низкой молекулярной массой, чем гемоглобин, масса которого составляет 68000 Да, и выводится из крови в 5 раз быстрее (Верболович П.А., 1961).
ОПН возникает лишь в 50% случаев краш-синдрома. Степень блокады почечных канальцев миоглобином и тяжесть ОПН часто не соответствуют друг другу (Насонкин О.С., Криворучко Б.И., 1991).
Предполагается, что путем искусственной элиминации продуктов миолиза можно существенно улучшить патофизиологическую ситуацию при рабдомиолизе, предотвратить или даже добиться обратного развития вторичных органных изменений. Тем не менее, интенсивный плазмообмен не влияет на ОПН, продолжительность периода олигурии или сроки восстановления функции мышц (Тимохов В.С. с соавт., 1997). Введение животным в опыте миоглобина не вызывает ОПН, ее можно достичь в эксперименте лишь при снижении рН мочи ниже 6,0, чего в реальных условиях не бывает.
В эксперименте в изолированной почке крысы при нормальном рН миоглобин в концентрации 25–250 мг/дл в минимальной степени нарушал перфузию почки, скорость фильтрации в клубочках и канальцевую реабсорбцию натрия. В отличие от этого, при рН 7,1 миоглобин вызывал вазоконстрикцию, снижение клубочковой фильтрации и канальцевой реабсорбции натрия и увеличивал гипоксическое повреждение эпителия в нисходящей части нефрона (Heyman S.N. С соавт., 1997) .
Ни гемодиализ, ни плазмообмен, ни длительная гемодиафильтрация, позволяющие компенсировать острую почечную недостаточность и обеспечивающие выживание больных с краш-синдромом, не ускоряют выведение миоглобина с мочой, что также дает основание усомниться в его роли в патогенезе ОПН.
Гиперкалиемия
Считается, что подвергшаяся раздавливанию мышечная ткань теряет до 66% содержащегося в ней калия. Именно фактор гиперкалиемии за счет нарушений сердечного ритма служит непосредственной причиной смерти, наступающей при резкой декомпрессии, как это бывает при снятии с конечности длительно сдавливавшего ее жгута. J.Oda с соавторами (1997) указывают на гиперкалиемию и гиповолемию как на непосредственную причину смерти в первые 5 суток от момента травмы 50 умерших из числа 372 госпитализированных с краш-синдромом. Однако известно, что такое развитие патологического состояния наблюдается далеко не всегда. Возможно, что в ряде случаев выход калия из поврежденных клеток происходит более постепенно.
Плазмопотеря
При СПС объем скапливающей в поврежденных тканях воды может достигать 6–10 л, однако перераспределение воды в организме и увеличение гематокрита при этом состоянии не столь выражены, как при краш-синдроме. При последнем плазмопотеря может достигать 30% от объема циркулирующей крови (Кузин М.И., 1985).
По данным Б.В.Кравцова и Л.П.Чипко (1973), спустя 4 часа с момента сдавления объем циркулирующей плазмы становится ниже исходной величины более чем на 40%. Уменьшается на 38,5% и объем циркулирующих эритроцитов. При этом скорость тока крови в магистральных сосудах снижается в 2 раза.
При краш-синдроме в ряде случаев нарушается также и целостность крупных сосудов, особенно при переломах крупных костей, при этом объем крови, излившейся в мягкие ткани, может достигать 30–40% от общего объема циркулирующей в организме крови. Снижение ОЦК за счет развития SIRS.
Введение в первые двое суток госпитализации менее 10л растворов является одним из двух факторов, обеспечивающих развитие при краш-синдроме ОПН.
Тканевой тромбопластин
Уже при длительности компрессии 15–60 минут у животных возникают явления гиперкоагуляции с активным потреблением тромбина и фибриногена с уменьшением числа циркулирующих тромбоцитов за счет коагулопатии потребления. Гиперкоагуляция сопровождается развитием ДВС-синдрома, характерного для краш-синдрома (Huerta-Alardin A.L. et al., 2005), что проявляется повышенной кровоточивостью и множественными кровоизлияниями.
При лечении 12 пострадавших в результате землетрясения в Армении, в 4 случаях отмечали тяжелые носовые кровотечения, в 3 — маточные, одно из которых оказалось смертельным, в 5 — кровотечения из острых эрозий желудка, а также множественные кровоизлияния в коже, слизистой оболочке губ и десен (Михайлов А.А. с соавт., 1991).
Активация ПОЛ
В норме свободнорадикальные формы кислорода детоксицируются в клетке эндогенными ферментами, которые катализируют супероксидный радикал в кислород и перекись водорода, а последняя за счет каталазы и пероксидазы превращается в воду и кислород. Как показали исследования (Нечаев Э.А. с соавт., 1993), при острой ишемии возникает повреждение ферментных систем и структур клеточных мембран, в результате чего происходит накопление перекисей и свободных радикалов при одновременном снижении антиоксидантной активности тканей, находящихся в условиях ишемии.
В эксперименте продемонстрировано повышение содержания продуктов ПОЛ как в раздавленных мышцах, так и в крови и в миокарде. В частности, содержание диеновых конъюгатов в течение 6 часов после декомпрессии было повышено в 5 раз, эта концентрация сохранялась на протяжении 3 суток, а далее снижалась, оставаясь повышенной до 6 суток (Кулиева А.А.,1990) . Содержание малонового диальдегида характеризовалось той же динамикой при повышении его содержания в исследованных тканях в 2,7 раза. Концентрация суммарных гидроперекисей липидов нарастала в течение 24 часов и в дальнейшем снижалась после 4 суток.
Аритмия
Среди веществ, выделяющихся при активации ПОЛ, ряд соединений обладает аритмогенным действием на миокард. К таким веществам относятся лизофосфоглицериды, которые представляют собой продукты деградации клеточных мембран и представлены двумя формами — лизофосфатидил-холином и лизофосфатидилэтаноламином.
Продемонстрировано в эксперименте (Corr P.B. с соавт.,1982), что внутривенное введение собакам лизофосфоглицеридов вызывает острые нарушения сердечного ритма вплоть до развития фибрилляции желудочков.
Функция почек
Гиповолемия, нарушения системного кровотока, спазм кортикальных сосудов, вызванный выбросом вазопрессина из гипофиза, уже в компрессионном периоде увеличивают реабсорбцию воды в почечных канальцах и приводят к олигурии. Возрастание выделения альдостерона повышает реабсорбцию натрия и снижает клубочковую фильтрацию, приводя к задержке воды и отеку почечной паренхимы (Симбирцев С.А., Шрайбер М.Г., 1978) и развитию десквамативно-обструктивной нефропатии. Повышение интерстициального давления, сопровождающееся нарушением оттока венозной крови, в свою очередь, должно еще больше усиливать отек интерстиция — возникает своего рода порочный круг.
Опыт со сдавлением мягких тканей у собак показал (Тройняков Н.К., 1977), что уже в периоде компрессии клубочковая фильтрация снижалась с 57,35±7,6 мл/мин. до 23,22±3,5 мл/мин (p<0,05).
Мышцы
При сдавлении мышц в течение 4 часов и более в них уже наблюдаются явления деструкции вплоть до их распада. Если же при компрессии происходит раздавливание тканей, то необратимые изменения могут наблюдаться в них уже через 5–20 минут (Горячев А.Н., Туршева И.Г., 1978). Примечательно, что, по данным В.И.Рудаева с соавторами (1999) до реперфузии выявить изменения в мышцах невозможно.
Конечность всегда отечна и не только в зоне ран, если таковые имеются. В отличие от анасарки ткани на ощупь упруги, и при надавливании на них не остается вдавлений от пальцев. В большинстве случаев кожа даже вне области сдавления имеет обычно багрово-синюшную окраску, имеются кровоподтеки. Даже вне зоны сдавления эпидермис бывает отслоенным в виде лоскутов.
Для умерших в ближайшую неделю после травмы характерно преобладание в миоцитах колликвационного некроза над коагуляционным по дискоидному типу, нарастание отека, лизис миофиламентов, появление уже через 3 дня после травмы очагов обызвествления по периферии зоны некроза наряду с проявлениями демаркационного воспаления с участием макрофагов.
В более поздние сроки Л.Н. Зимина с соавторами (1998) отмечали «застывание» очагов некроза: даже по прошествии 6,5 месяцев в конечностях сохранялись участки некротизированной ткани, не подвергшейся резорбции и реституции или субституции. В отношении отдаленных последствий сдавления конечности у выживших известно, что полноценного восстановления функции не происходит.
Макроскопические изменения
- В полостях обилие серозной жидкости, окрашенной кровью.
- В серозных оболочках очаговые кровоизлияния.
- Острые язвы и эрозии в желудке.
- При ОПН почки массой ≥ 400г, корковое вещество бледно-серое, набухшее, мозговое — темно-красное с бурыми радиальными полосками.
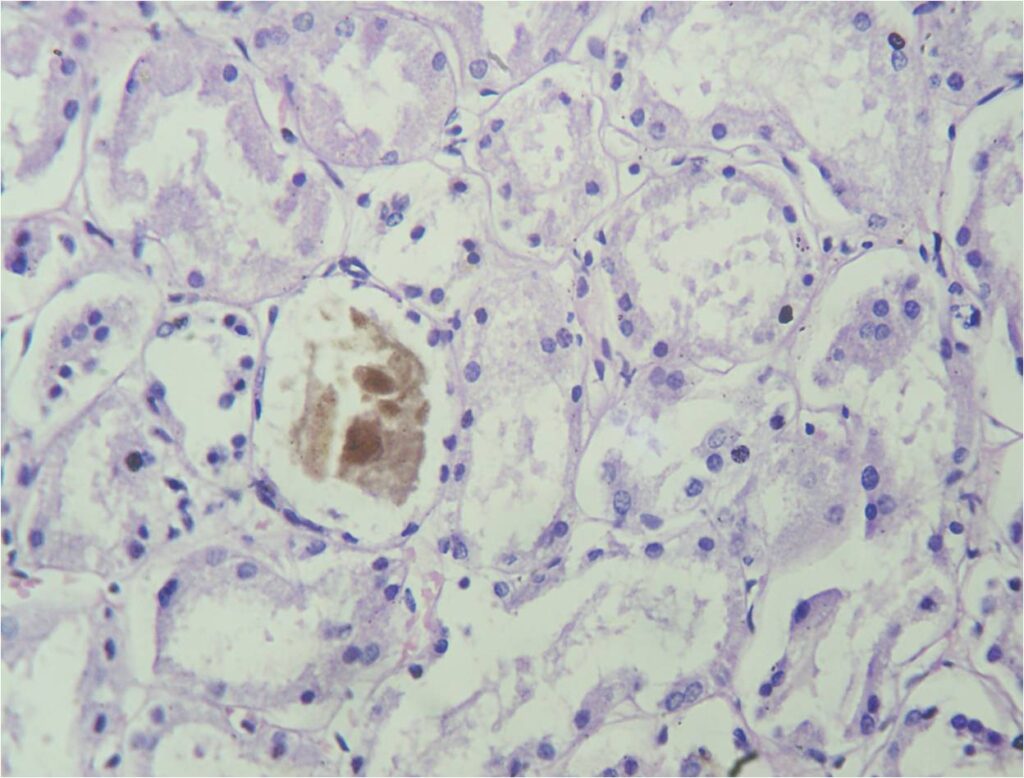
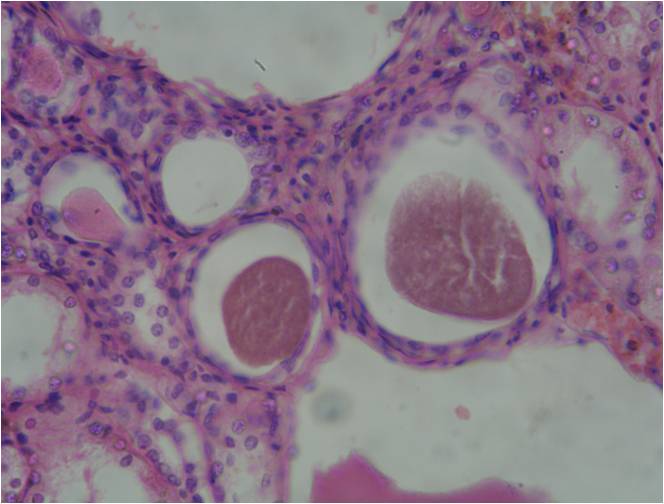
Из числа расширенных за счет обтурации почечных канальцев только некоторые закупорены пигментными цилинд-рами, дающими положи-тельную реакцию по Лепене, как и гемоглобин, в то время как просвет других бывает перекрытым плотными белковыми массами, но не пигментированными.
Пигментный нефроз
Наблюдается выделение жидкого пигмента по системе нефрона с частичным его поглощением эпителием проксимальных канальцев, что подтверждается данными других авторов, обнаруживавших при электронно-микроскопическом исследовании вакуоли с осмиофильным содержимым, соответствующим миоглобину.
На 5–10 сутки обнаруживаются дистрофические и некробиотические изменения эпителия проксимальных канальцев с отторжением его в просвет канальцев в виде крупных глыбок с формированием зернистых цилиндров. Организация пигментных цилиндров к 10-28 суткам (Н.К. Пермяков, 1951).
Непосредственные причины смерти
- Сепсис 17,3±2,5 суток. Факторы риска: женский пол, низкое АД при поступлении, активность креатинкиназы сыворотки крови >20000 U/l и наличие множественных повреждений с вовлечением области груди и живота (Ersoy A. et al., 2003).
- Обострение имевшихся до катастрофы заболеваний.
- ОПН на 1-2 неделе, далее – пневмония, панкреонекроз, сепсис НИИ СП им.Склифосовского).
- Гиперкалиемия выше 7 mEq/l (связь скорее косвенная).
Патологические изменения
Сдавленная конечность резко отечна, кожные покровы бледные, с большим количеством ссадин и кровоподтёков. Подкожная жировая клетчатка и мышцы пропитаны отёчной жидкостью желтоватого цвета. Мышцы имбибированы кровью, имеют тусклый вид, целостность сосудов не нарушена. При микроскопическом исследовании мышц выявляется характерная картина восковидной дегенерации . Наблюдается отёк головного мозга. Лёгкие застойно-полнокровные, иногда имеются явления отёка и пневмонии. В миокарде – дистрофические изменения. В печени и органах ЖКТ отмечается полнокровие с множественными кровоизлияниями в слизистую оболочку желудка и тонкой кишки.
Наиболее выражены изменения в почках: почки увеличены на разрезе, выражена резкая бледность коркового слоя. В эпителии извитых канальцев дистрофические изменения. В просвете канальцев содержатся зернистые и мелкокапельные белковые массы. Часть канальцев полностью закупорена цилиндрами миоглобина.
Дифференциально-диагностические признаки синдрома сдавления и травматического шока.
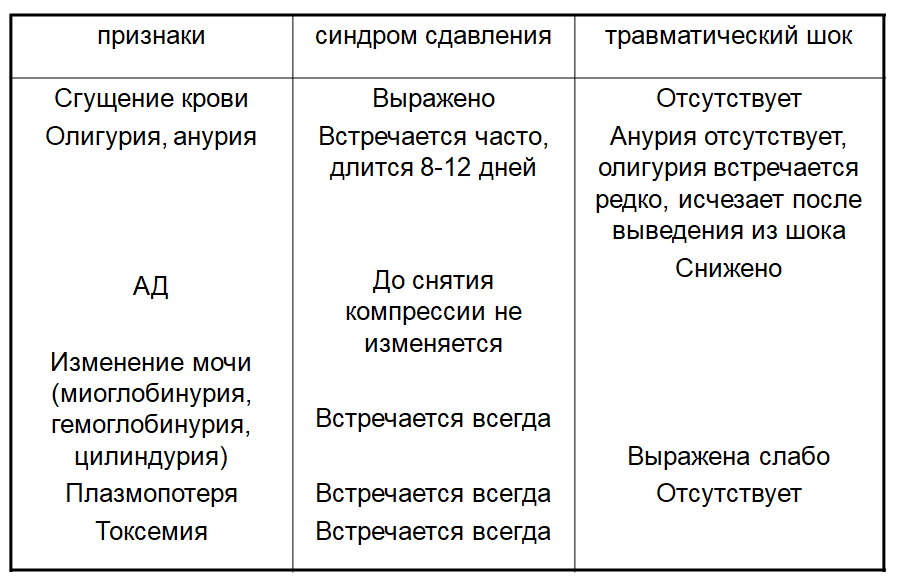
Клиническая картина
I период – 24-48ч после освобождения от сдавления. Травматический шок: болевые реакции, эмоциональный стресс, непосредственные последствия плазмо- и кровопотери. Возможно развитие гемоконцентрации, патологических изменений в моче, повышение остаточного азота крови.
Для синдрома сдавления характерен «светлый промежуток», который наблюдается после оказания медицинской помощи. Однако состояние пострадавшего вскоре начинает вновь ухудшаться и развивается II период, или промежуточный.
II период (промежуточный) – С 3-4 по 8-12 день – развитие, прежде всего, почечной недостаточности. Отёк освобождённой конечности продолжается, образуются пузыри, кровоизлияния. Конечность приобретает такой же вид, как при анаэробной инфекции. Обнаруживается прогрессирующая анемия, гемоконцентрация сменяется с гемодилюцией, уменьшается диурез, растёт уровень остаточного азота. Летальность может достигать 35%.
III период (восстановительный) – Начинается обычно с 3-4 недели болезни. На фоне нормализации функции почек, положительных сдвигов в белковом электролитном балансе остаются тяжёлыми изменения со стороны поражённых тканей. Это обширные язвы, некрозы, остеомиелит, гнойные осложнения со стороны суставов, флебиты, тромбозы и т.д.
Существуют 4 клинические формы синдрома длительного сдавления (М. И. Кузин):
- Лёгкая, длительность сдавления сегментов конечности не превышает 4 часа.
- Средняя – сдавление всей конечности в течение 6 ч. В большинстве случаев нет выраженных гемодинамических расстройств, функция почек страдает сравнительно мало.
- Тяжёлая форма возникает вследствие сдавления всей конечности 7-8 ч, отчётливо проявляется симптоматика почечной недостаточности и гемодинамические расстройства.
- Крайне тяжёлая форма развивается, если сдавлению подвергаются обе конечности в течение 6 ч и более. Пострадавшие умирают в течение первых 2-3 суток
Лечение на этапах медицинской эвакуации

Первая помощь. Освобождая пострадавшего от сдавления, необходимо наложить жгут проксимальнее места сдавления и туго забинтовать конечность для предупреждения отёка.
Желательно осуществить гипотермию конечности (предупреждение развития гиперкалиемии).
Обязательны иммобилизация, введение обезболивающих и седативных средств.
Первая врачебная помощь (ПМП) – Производятся новокаиновую блокаду – 200-400 мл тёплого 0,25% раствора проксимальнее места наложения жгута, после чего жгут медленно снимают. Полезнее раствора новокаина ввести антибиотики широкого спектра действия. Пострадавшему делают двустороннюю паранефральную блокаду, вводят столбнячный анатоксин. Охлаждение конечности с тугим бинтованием следует продолжать. Вместо тугого бинтования показано использования пневматической шины для иммобилизации переломов. В этом случае будет одновременно осуществляться и равномерная компрессия конечности, и иммобилизация. Вводят наркотики и антигистаминные препараты, сердечно-сосудистые средства. Дают щелочное питьё и горячий чай.
Квалифицированная хирургическая помощь. Пострадавших с синдромом сдавления следует задерживать в медсанбате только в том случае, если у них комбинированное поражение и требуется хирургическая помощь профиля медсанбата. Для борьбы с ацидозом в\в вводят 3-5% раствор натрия бикарбоната 300-500мл, назначают большие дозы (15-25г в день) цитрата натрия.Показано также питьё больших количеств щелочных растворов, применение высоких клизм с бикарбонатом натрия. Для уменьшения спазма сосудов коркового слоя почек целесообразны в\в капельные вливания 0,1% раствора новокаина (300 мл). В течение суток вводят в вену до 4 л жидкости. В составе жидкости должно быть 1-1,5 л 5% раствора глюкозы и инсулина в соответствующих дозах.Если у пострадавшего развивается симптоматика гемоконцентрации, то производится инфузионная терапия с применением кристаллоидных и низкомолекулярных плазмозаменителей. Производят фасциотомию.
Специализированная хирургическая помощь. При гиперкалиемии в\в вводят 50-60 мл 10% раствора глюконата кальция, 200-300 мл 5% раствора глюкозы, оксибутират натрия. Для нейтрализации аммиака необходимо введение глютаминовой кислоты и желатина. При продолжающейся в течении 2-3дней олигурии применяют экстракорпоральный гемодиализ. У пострадавших с синдромом длительного сдавливания нередко возникают показания к ампутации конечностей. Следует помнить, что ампутацию надо выполнять до развития анурии.